Covid-19
Anvisa aprova medicamento que reduz risco de morte em até 89%

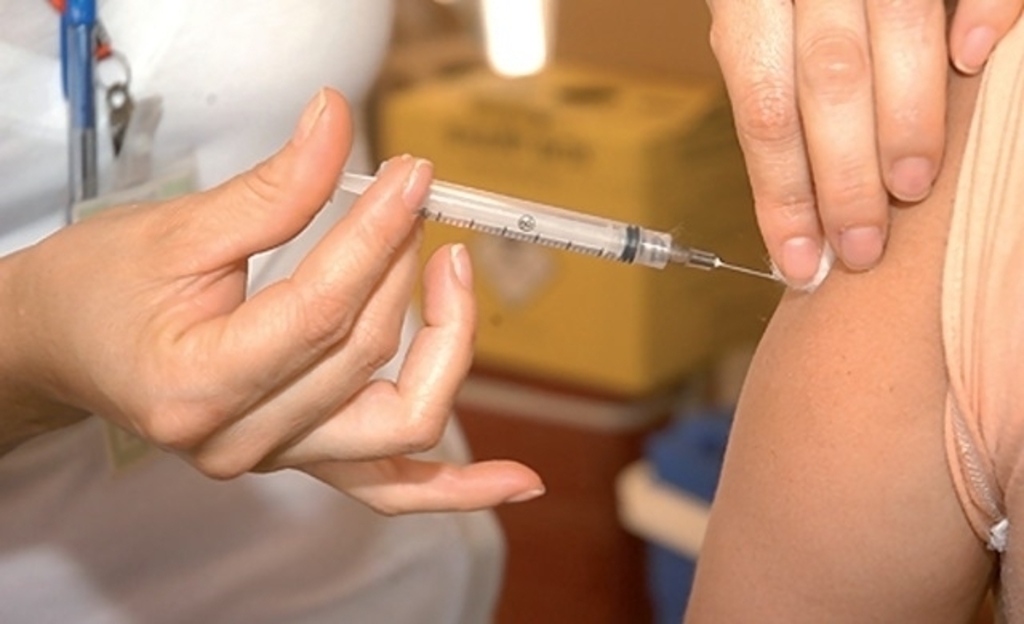
Ilustração -
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, na quarta-feira, 4/5, o uso emergencial do antiviral oral contra a covid-19 em grupos específicos. O molnupiravir, também conhecido pelo nome comercial Lagevrio, é desenvolvido pela farmacêutica Merck Sharp & Dohme (MSD) e apresentou resultados de ser capaz de reduzir em 89% o risco de morte por covid-19. A empresa tem expectativa de que o medicamento esteja disponível no Sistema Único de Saúde (SUS) no início de julho.
A distribuição do medicamento no país será de responsabilidade da Fundação Oswaldo Cruz (Fiocruz), que fechou um acordo de cooperação tecnológica com a MSD nesta quinta-feira, 5/5. Agora, falta somente a avaliação da Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde (Conitec).
De acordo com o diretor da Unidade de Negócios de Infectologia da MSD no Brasil, Mario Ferrari, apesar de não haver uma data certa para o remédio estar disponível no país, a empresa tem a expectativa de que seja em algumas semanas. A estimativa do Diretor leva em conta os prazos da Conitec para analisar outras tecnologias e medicamentos no contexto da covid-19, que foram mais rápidos do que tradicionalmente ocorre com doenças diferentes.
O medicamento foi aprovado para uso em pessoas que mesmo vacinadas tenham risco de desenvolver quadros graves da covid-19. Esse é o caso de pacientes oncológicos, portadores do vírus HIV, transplantados ou imunossuprimidos. O Ministério da Saúde definirá quais grupos serão aptos a receber o remédio pelo SUS, o que impacta também na quantidade de tratamentos a ser encomendada.
Até o momento, a farmacêutica já produziu 10 milhões de tratamentos em 2021 ao redor do globo terrestre e está fabricando mais 20 milhões neste ano. Porém, o foco da empresa neste momento é fornecer o medicamento somente para o SUS.
O medicamento foi desenvolvido por uma empresa de biotecnologia dos EUA sem fins lucrativos - a Drug Innovations at Emory - que recebe financiamento parcial do governo norte-americano. Posteriormente, a fórmula foi licenciada pela empresa Ridgeback Biotherapeutics, sediada na Flórida, que firmou acordo com a MSD para viabilizar os estudos clínicos e a produção.
Os testes avançaram para a fase final em abril de 2021, após resultados promissores em voluntários que fizeram uso do medicamento nos primeiros dias desde o início dos sintomas. O pedido de uso emergencial na Anvisa foi protocolado em 21 de novembro. O molnupiravir já foi aprovado por importantes agências reguladoras, como a dos Estados Unidos, do Reino Unido, da União Europeia e do Japão, e já está em uso em 17 países.
Os resultados mostraram que o molnupiravir foi capaz de reduzir em 89% o risco de morte por covid-19 quando comparado à substância que não causa efeito no organismo. O antiviral se apresentou eficaz em pacientes infectados por variantes mais recentes do coronavírus, que escapam da proteção conferida pelas vacinas.
















Deixe seu comentário